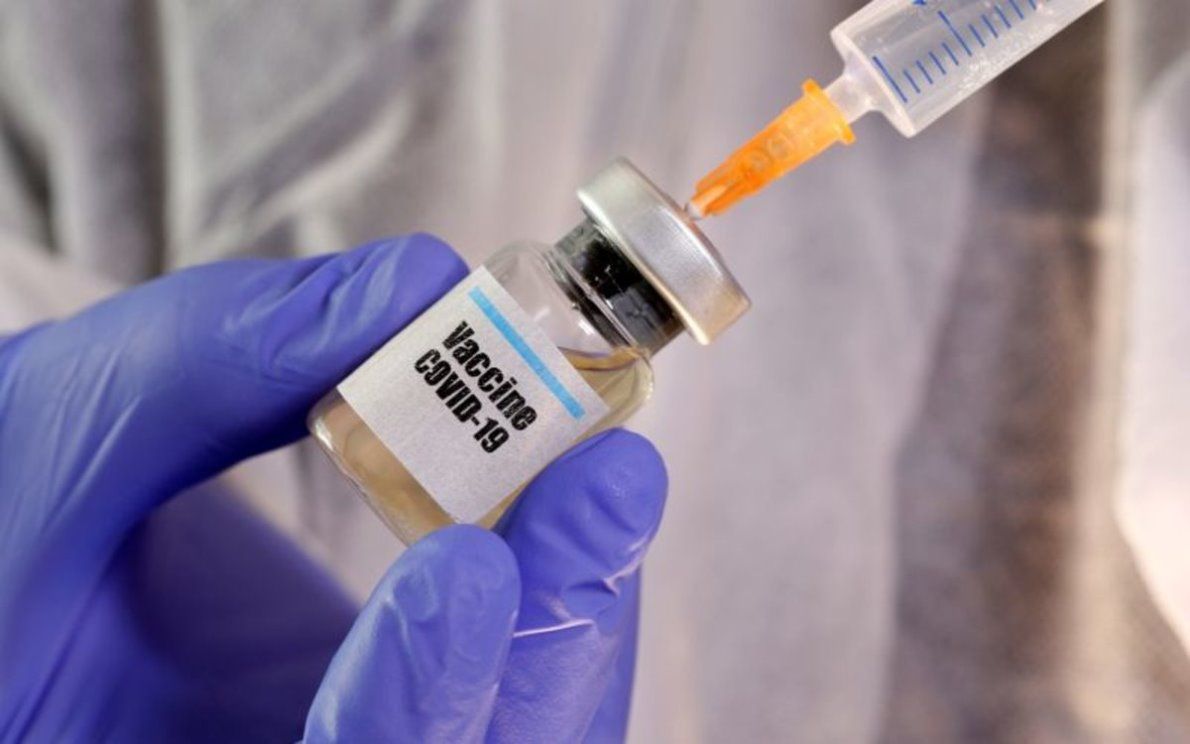
Según informa la web especializada Diario Médico, la compañía Pfizer y su socia BioNTech enviaron el pasado día 20 de noviembre, una petición para la autorización de emergencia a la FDA (organismo regulador del medicamento de Estados Unidos) y así comenzar la distribución de su vacuna contra la covid-19 que, según sus propias investigaciones, ha demostrado hasta un 95% de eficacia en pruebas clínicas preliminares, y que podría aplicarse a población de riesgo a partir del mes de diciembre.
Paso a paso
La Agencia de Alimentos y Medicamentos de Estados Unidos (FDA) tendría que revisar al menos dos meses de datos de respuesta de los voluntarios a la vacuna, así como comprobar su seguridad en niños, personas mayores y racialmente diversas, pero la urgencia del proceso podrían reducir estas pruebas a tan solo semanas para que la primera vacuna estadounidense contra la covid-19 esté disponible cuanto antes.
Más peticiones
Los laboratorios Pfizer y la filial alemana BioNTech están en vías de presentación de la petición de autorizaciones similares a los organismos reguladores de Australia, Canadá, Japón, Reino Unido y la Unión Europea, donde el aumento de casos podría haber rebasado ya el pico más alto de su ciclo infeccioso.
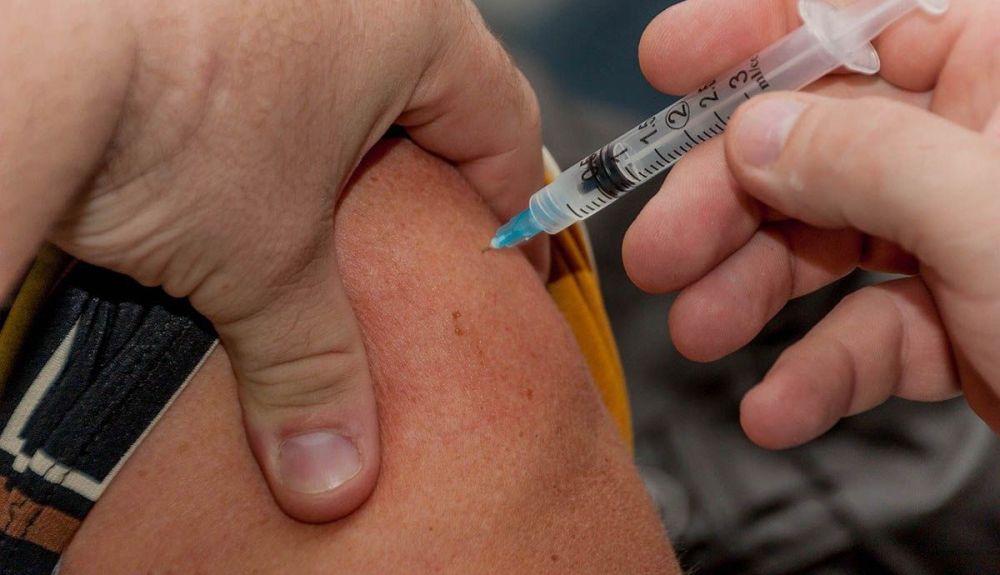
En fase III
Los últimos datos publicados de la fase III de pruebas clínicas de esta vacuna se basan en el estudio de 43.661 voluntarios, 41.135 de los cuales recibieron las dos dosis de las que consta la vacuna en centros de pruebas en Estados Unidos, Alemania, Turquía, Sudáfrica, Brasil y Argentina. El índice de eficacia es del 95% en general y del 94% entre mayores de 65 años (población de riesgo), y por lo tanto es muy superior al 50% que exige la FDA para aprobar candidatas a vacunas contra la covid-19.
La eficacia eficacia de la vacuna se han conseguido tras el contagio con covid-19 de 170 voluntarios, mientras que los datos de seguridad y efectos secundarios se han obtenido de los resultados de 8.000 participantes aleatorios y por el seguimiento dado a la mayoría de los que han recibido dos dosis de la llamada BTN162b2.
Los datos de seguridad incluyen la respuesta en 100 niños entre 12 y 15 años, y más de un 40% de personas de diversos orígenes étnicos y raciales, así como un 41% de edades comprendidas entre 56 y 85 años.